![]()
I Childhood Stroke
![]()
1 Pediatric Clinical Scouts – PCS
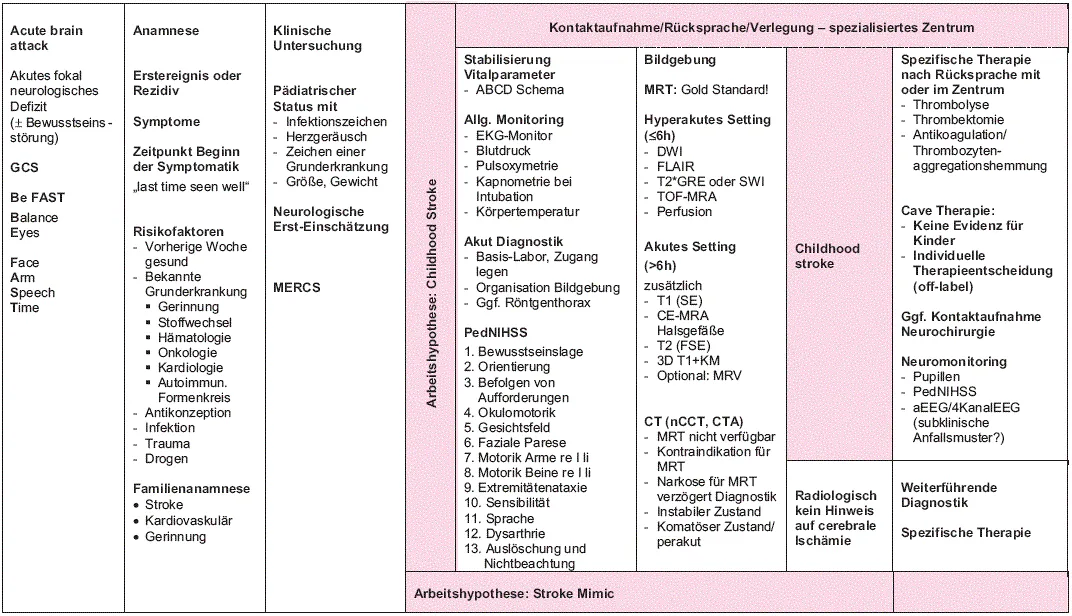
1.1 PCS – akut
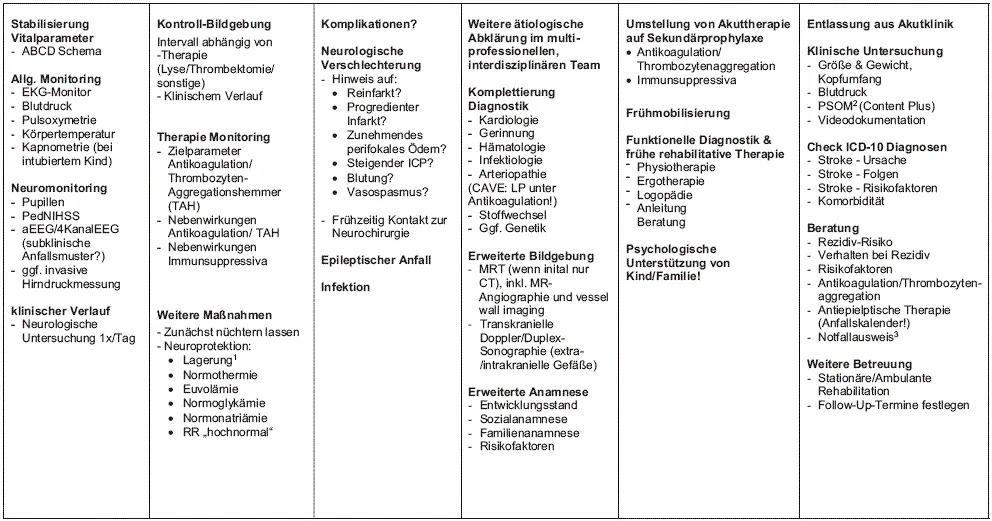
1.2 PCS – postakut
1 Lagerung zur Hirndruckprophylaxe: achsengerecht, Kopfmittellage, Oberkörper max. 30° hochgelagert (je nach Situation)
2 PSOM Pediatric Stroke Outcome Measure
3 Notfallausweis mit folgenden Angaben: Z.n. Stroke, Angaben zur Antikoagulation, Verhalten bei Rezidiv, Verhalten bei Trauma unter Antikoagulation, Notfallmedikation für epileptischen Anfall, Kontaktdaten des behandelnden Zentrums!
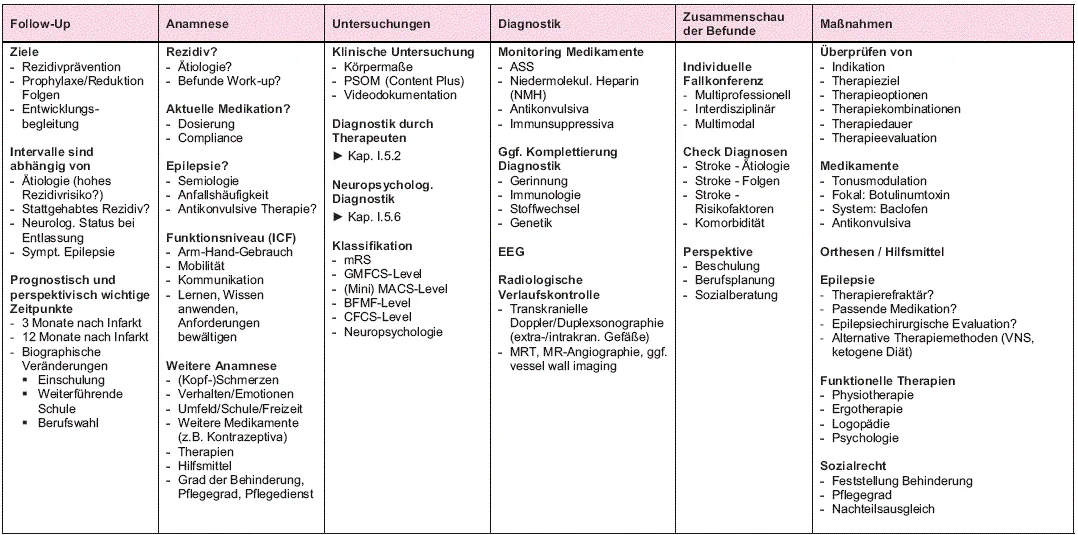
1.3 PCS – chronisch
PSOM: Pediatric Stroke Outcome Measure, mRS: modified Rankin Scale, GMFCS: Gross Motor Function, CFCS: Communication Classification System, MACS: Manual Ability Classification System, BFMF: Bimanual Fine Motor Function Eine ausführliche Darstellung der empfohlenen Assessments und Evaluationsinstrumente findet sich im Content plus.
![]()
2 Einführung
2.1 Epidemiologie
Lucia Gerstl
Der Schlaganfall im Kindesalter zählt mit einer Inzidenz von 1–8/100.000 pro Jahr zu den per definitionem seltenen Erkrankungen. Er ist gekennzeichnet durch eine hohe Morbidität (nur ca. 1/3 der betroffenen Kinder erholen sich vollständig) und Mortalität (childhood stroke ist eine der zehn häufigsten Todesursachen im Kindesalter). Die »Global Burden of Disease Study 2010« registrierte weltweit einen Anstieg der Inzidenz im Kindes- und Jugendalter.
Die Altersverteilung zeigt in verschiedenen Studien Peaks im 1. Lebensjahr und Vorschulalter und einen weiteren Peak in der Adoleszenz. Aufgrund bestehender Versorgungsstrukturen mit Aufnahme adoleszenter Patienten auf Stroke Units in (erwachsenen) neurologischen Kliniken ist wahrscheinlich von einem »underreporting« in den Studien zum kindlichen Schlaganfall und damit von einer höheren Inzidenz in der Adoleszenz auszugehen.
Die Geschlechterverteilung zeigt eine bislang nicht erklärbare leichte Knabenwendigkeit bis zu 1,5:1, u. a. werden ein möglicher Einfluss des endogenen Testosterons wie auch eine neuroprotektive Wirkung des Östrogens diskutiert.
Literatur
Feigin VL, Forouzanfar MH, Krishnamurthi R, Mensah GA, Connor M, Bennett DA, Moran AE, Sacco RL, Anderson L, Truelsen T, O’Donnell M, Venketasubramanian N, Barker-Collo S, Lawes CM, Wang W, Shinohara Y, Witt E, Ezzati M, Naghavi M, Murray C, Global Burden of Diseases, Injuries, and Risk Factors Study 2010 (GBD 2010) and the GBD Stroke Experts Group (2014) Global and regional burden of stroke during 1990-2010: findings from the Global Burden of Disease Study 2010. Lancet 383:245-254.
Fullerton HJ, Wu YW, Zhao S, Johnston SC (2003) Risk of stroke in children: ethnic and gender disparities. Neurology 61:189-194.
Gerstl L, Weinberger R, von Kries R, Heinen F, Schroeder AS, Bonfert MV, Borggraefe I, Tacke M, Vill K, Landgraf MN, Kurnik K, Olivieri M (2018) Eur J Paediatr Neurol. 22: 380-386.
Golomb MR, Fullerton HJ, Nowak-Gottl U, Deveber G, International Pediatric Stroke Study Group (2009) Male predominance in childhood ischemic stroke: findings from the international pediatric stroke study. Stroke 40:52-57.
Lynch JK, Hirtz DG, DeVeber G, Nelson KB (2002) Report of the National Institute of Neurological Disorders and Stroke workshop on perinatal and childhood stroke. Pediatrics 109:116-123.
2.2 Ätiologie und Risikofaktoren
2.2.1 Arteriopathien
Maja Steinlin
Arteriopathien bekommen eine zunehmende Bedeutung beim kindlichen ischämischen Schlaganfall. Sie sind bei knapp der Hälfte der kindlichen Schlaganfälle einer der bedeutendsten Risikofaktoren.
Arteriosklerose macht bei den Erwachsenen ca. 95% der Arteriopathien aus, kommt jedoch im Kindesalter praktisch nicht vor. Die bedeutendste Arteriopathie im Kindesalter ist die transiente fokale Arteriopathie (ca. 30%) gefolgt von Dissektionen und Moyamoya (je ca. 10%). In den letzten Jahren werden zunehmend spezifische Arteriopathien mit einem genetischen Hintergrund beschrieben. Die Vielfältigkeit der Arteriopathien im Kindesalter macht eine sorgfältige Diagnosestellung erforderlich. Für die Abgrenzung einzelner Differentialdiagnosen ist die Gefäß-Bildgebung mitentscheidend. Neben der Basisinformation durch MR-Angiographie (TOF oder contrast enhanced) helfen spezielle Gefäßwand-Bildgebungen, wie z. B. dark blood imaging, verbesserte Information über die zu Grunde liegende Pathologie zu erhalten. Eine sorgfältige Familienanamnese weist auf mögliche genetische oder infektiologische Ursachen hin, eine sorgfältige klinische Untersuchung hilft durch zusätzliche Befunde (v.a. auch der Haut) weiter.
Die korrekte Diagnose der Ursache der Arteriopathie ist frühestmöglich zu stellen, um die richtige Therapie in die Wege leiten zu können, aber auch um das Wiederholungsrisiko besser abschätzen zu können.
2.2.1.1 Transiente fokale Arteriopathie (TFA) (häufig synonym verwendet: FCA= focal cerebral arteriopathy; TCA= transient cerebral arteriopathy)
Die transiente fokale Arteriopathie (TFA) stellt die häufigste Arteriopathie im Kindesalter dar. Sie ist bedingt durch eine transiente parainfektiöse inflammatorische Veränderung der Gefäßwand.
Ätiologie, Histologie und Bildgebung
Die Varizellen-Arteriopathie ist die bekannteste Ursache: Wochen bis einige Monate nach der akuten Varizellen-Infektion kommt es höchstwahrscheinlich durch Reaktivierung des Virus zu einer inflammatorischen Reaktion der Gefäßwand. In verschiedenen histologischen Untersuchungen und Autopsiefällen konnten Mastozyten und Lymphozyten und vereinzelt auch Varizellenviren in der Gefäßwand nachgewiesen werden. Durch die inflammatorische Reaktion kommt es zur Schwellung der Gefäßwand und dadurch zur Verengung bis/oder zum Verschluss des Gefäßes.
Andere infektiöse Erreger wie Herpes simplex, Borrelien, Mycoplasmen, Enteroviren oder Parvoviren kommen ursächlich ebenfalls in Frage.
Am häufigsten ist das Segment M1 der A. cerebri media betroffen, vereinzelt auch das Segment A1 oder die distalen Anteile der A. carotis interna, was zum sogenannten T-Verschluss führt. Aber auch TFA im hinteren Strombereich sind bekannt. In der Bildgebung kann neben der Stenose häufig auch die inflammatorische Gefäßwandreaktion durch Verdickung und Kontrastmittelanreicherung resp. Hyperintensität im dark blood imaging dargestellt werden.
Klinik
Klinisch zeigen diese Kinder eine akute fokale Ausfallssymptomatik entsprechend dem befallenen Gefäßterritorium. Vor allem die M1-Stenosen führen gerne zu einem stotternden Beginn der Symptome, wohl durch die zeitlich leicht verschobenen Ischämien in den vereinzelten lenticulostriatalen Arterien. In den ersten Tagen und Wochen kann noch eine Zunahme der Gefäßstenosierung auftreten, was zu einer klinischen Verschlechterung oder aber auch einem Rezidiv des Schlaganfalls führen kann. Rezidive treten in 5–18% in den ersten drei Monaten nach dem Schlaganfall auf und werden nach einem Jahr zur Seltenheit. Die Kinder erholen sich von den Symptomen, ca. 60% haben jedoch bleibende neurologische oder neurokognitive Probleme. In einer Gruppe von 73 europäisch-australischen Kindern zeigte sich im klinischen follow up ein mean PSOM (Pediatric Stroke Outcome Measure,
Content Plus) Wert von 0.5, aber mit einem breiten Ra...