Aufgrund der stetig wachsenden Zahl älterer Menschen rücken die Probleme der Betagten und Hochbetagten immer mehr in den Vordergrund der zahnärztlichen Tätigkeit. Die täglichen Erfahrungen in der zahnärztlichen Praxis lehren uns, dass ganz individuelle Lebenserfahrungen, erhebliche Unterschiede im Allgemeinzustand und uneinheitliche finanzielle Verhältnisses ältere Menschen zu einer extrem heterogenen Patientengruppe machen und der Umgang mit den Senioren allen Beteiligten oftmals ein hohes Maß an Wissen, Erfahrung und Toleranz abverlangt. Die Betagten und Hochbetagten benötigen oft umfangreiche Rehabilitation im stomatognathen System, wobei die Mundgesundheit jedoch nur ein Teilbereich ist, der zur Lebensqualität beiträgt. Dieses Buch bietet eine Zusammenstellung verschiedener multidisziplinär angelegter Kapitel, die dabei helfen soll, die komplexen, über die Zahnmedizin hinausgehenden Zusammenhänge besser zu verstehen. Zahlreiche Ratschläge und Tipps der einzelnen Autoren machen die täglich vom Zahnarzt abverlangten Entscheidungen in Zusammenarbeit mit den Betagten und Hochbetagten leichter.

- 320 Seiten
- German
- ePUB (handyfreundlich)
- Über iOS und Android verfügbar
eBook - ePub
Der alte Patient in der zahnärztlichen Praxis
Über dieses Buch
375,005 Studierende vertrauen auf uns
Zugang zu über 1 Million Titeln zu einem fairen monatlichen Preis.
Mit unseren Lerntools kannst du noch effizienter lernen.
Information
Thema
MedizinThema
Zahnmedizin

Einleitung
Aufgrund der demografischen Veränderungen der Bevölkerung in den Industrienationen und insbesondere in Deutschland werden kariöse Läsionen auf freiliegenden Wurzeloberflächen zu einem der häufigsten Probleme werden, mit denen der niedergelassene Zahnarzt konfrontiert sein wird. Die klassischen Konzepte der Kariestherapie lassen sich nicht ohne Weiteres auf die Therapie der Wurzelkaries übertragen, da die Defekte häufig so ausgedehnt sind, dass eine Kavitätenpräparation im herkömmlichen Sinne den Zahn übermäßig schädigen würde. Außerdem erschwert die Lokalisation der Defekte nahe dem Gingivalsaum, oder manchmal sogar mit subgingivaler Ausdehnung, die notwendige Trockenlegung und damit eine randdichte Restauration. Schließlich kann der ältere Patient oft keine ausreichende häusliche Plaquekontrolle in einer Qualität durchführen, die für die Vermeidung von Wurzelkaries notwendig wäre, wie die Abbildung 18-1 zeigt. Daher müssen die präventiven und therapeutischen Ansätze einerseits an die spezifischen Aspekte der Ätiopathogenese der Wurzelkaries und andererseits an die ggf. veränderten Möglichkeiten der betroffenen Patienten angepasst werden.
Charakterisierung der Defekte
Für den Praxisalltag stellen sich insbesondere folgende Fragen:
- • Wie häufig muss bei unseren Patienten mit Wurzelkariesläsionen gerechnet werden?
- • Welche Patienten weisen ein erhöhtes Risiko auf?
- • Unterscheidet sich die Ätiopathogenese von der der Schmelzkaries?
- • Welche präventiven und minimalinvasiven Therapiemaßnahmen sind klinisch erfolgreich?
- • Wie können ausgedehnte Defekte restauriert werden?
- • Wo liegen die Grenzen der Zahnerhaltung?
Für Deutschland liegen dank der Vierten Deutschen Mundgesundheitsstudie (DMS IV) des Instituts der Deutschen Zahnärzte (IDZ) repräsentative Daten vor29. Tabelle 18-1 zeigt, wie dramatisch die Wurzelkarieserfahrung in den letzten 10 Jahren zugenommen hat, während Tabelle 18-2 die Verteilung auf die verschiedenen Altersgruppen und die Geschlechter angibt.
Tab. 18-1 Vergleich der Häufigkeit der Karieserfahrung zwischen 1997 und 2006. Während die Schmelzkaries im Mittel leicht zurückgegangen ist, wurden deutlich mehr Patienten mit Wurzelkaries registriert. Von allen freiliegenden Zahnhälsen waren nun 17 % kariös erkrankt, also fast 50 % mehr als vor 10 Jahren
| DMS III: 1997 | DMS IV: 2006 | |
|---|---|---|
| DMFT* (max.: 28) | 23,6 | 22,1 |
| DT | 0,3 | 0,3 |
| MT | 17, 6 | 14, 1 |
| DMFS** (max.: 128) | 103 | 83 |
| Sanierungsgrad | 93 % | 95 % |
| Wurzelkaries | 15,5 % | 45 % |
| RCI*** | 12,6 % | 17 % |
* DMFT: decayed, missing or filled teeth.
** DMFS: decayed, missing or filled surfaces.
*** RCI: Root caries index: decayed root surfaces/exposed root surfaces.
** DMFS: decayed, missing or filled surfaces.
*** RCI: Root caries index: decayed root surfaces/exposed root surfaces.
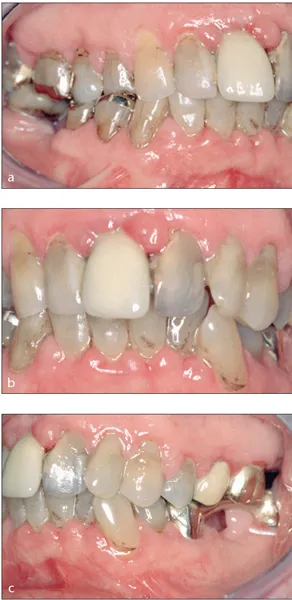
Abb. 18-1a bis c Klinisches Beispiel eines 80-jährigen Patienten, der zwar gesundheitsbewusst und motiviert ist, aber in der häuslichen Mundhygiene keine befriedigende Plaquebiofilmkontrolle erreichen konnte
Die Daten belegen die Faustregel, dass mindestens jede zehnte freiliegende Wurzeloberfläche unter dem Risiko steht, kariös zu erkranken. Anders als bei Schmelzkaries lässt sich kein systematischer Einfluss des Sozialstatus erkennen, wohingegen die Qualität der Mundhygiene als Risikofaktor epidemiologisch auffällig ist29. Die höhere Prävalenz im Alter ist aber nicht primär die Folge eines veränderten Ökosystems, auch wenn beispielsweise der Speichelmangel mit höherem Lebensalter zunimmt. Vielmehr steigt mit zunehmendem Alter die Anzahl an entblößten Wurzeloberflächen und damit das Wurzelkariesrisiko15. Bei Patienten mit aggressiven Parodontitiden und insbesondere bei Patienten während bzw. nach einer Parodontaltherapie haben Kariespathogene einen Selektionsvorteil, so dass die post operationem zugänglichen Wurzeloberflächen auch in einem früheren Lebensalter ein erhöhtes Risiko aufweisen33.
Wie viel empfindlicher freiliegende Wurzeloberflächen im Vergleich zum Schmelzmantel sind, zeigt ein Vergleich der kritischen pH-Werte. Auch wenn der Effekt in In-vitro-Studien wahrscheinlich überschätzt wird, konnte gezeigt werden, dass der kritische pH-Wert, bei dem freiliegendes Dentin in Lösung geht, bereits im Bereich zwischen 6,0 und 6,8 liegt, während Schmelz erst bei einem Säureangriff mit pH-Werten von 5,5 bis 5,7 demineralisiert wird17. Hinzu kommen noch strukturelle Unterschiede zwischen koronalem Dentin und Wurzeldentin. Wurzeldentin besitzt weniger und engere Dentinkanälchen und ist stärker mineralisiert, was zu unterschiedlichen Ausbreitungsrichtungen von Bakterien und verschiedenen histologischen Erscheinungsformen führen kann35,-37. Aufgrund des höheren organischen Anteils kommt es im Vergleich zu Schmelzkaries auch zu einem veränderten klinischen Erscheinungsbild.
Klinisch findet man unterschiedliche Defektformen von flächenhaften, stark erweichten kariösen Läsionen bis hin zu klar umschriebenen, dunkel verfärbten, harten Läsionen. Die Defekte sind häufig unterhalb der Schmelz-Zement-Grenze zu finden, können aber an allen exponierten Wurzeloberflächen – auch subgingival in einer Zahnfleischtasche – auftreten. Im Praxisalltag kann man zu dem Eindruck gelangen, dass bei dunkelbraun bis schwarz verfärbten Defekten der kariöse Prozess eher zum Stillstand gekommen ist, wohingegen aktive Defekte lediglich gelb bis hellbraun verfärbt sind und eine weiche, häufig mit Plaque bedeckte Oberflächenstruktur aufweisen31. Allerdings konnte in klinischen Studien und anhand von Untersuchungen des Infektionsgrades der Defektoberflächen gezeigt werden, dass der Grad der Verfärbung kein valides Kriterium darstellt42. Allein die Oberflächentextur (Härte) und der Abstand zum Gingivalsaum korrelieren mit dem Infektionsgrad, so dass lediglich die erweichte Wurzeloberfläche und eine Ausdehnung der Defekte bis zur Gingiva als Zeichen einer aktiven Läsion gewertet werden können27 (Abb. 18-2a und b).
| Alter | Gesamt | DOst | DWest | Männer | Frauen |
|---|---|---|---|---|---|
| 35-44 J.: Prävalenz | (n = 925) 21,5 % | (n = 170) 28,9 % | (n = 755) 19,9 % | (n = 471) 25,9 % | (n = 454) 17 % |
| 35-44 J.: RCI | (n = 580) 8,8 % | (n = 115) 11,2 % | (n = 464) 8,2 % | (n = 305) 10,2 % | (n = 275) 7,2 % |
| 65-74 J.: Prävalenz | (n = 1040) 45 % | (n = 214) 52,4 % | (n = 826) 43,1 % | (n = 480) 46,8 % | (n = 560) 43,5 % |
| 65-74 J.: RCI | (n = 712) 17 % | (n = 155) 15,2 % | (n = 557) 17,5 % | (n = 351) 16,5 % | (n = 361) 17,4 % |
Tab. 2 Angegeben ist die Häufigkeit von Wurzelkariesläsionen für Erwachsene und Senioren nach Alter und Geschlecht differenziert. Der RCI gibt an, wie viel Prozent der freiliegenden Wurzeloberflächen kariös erkrankt sind
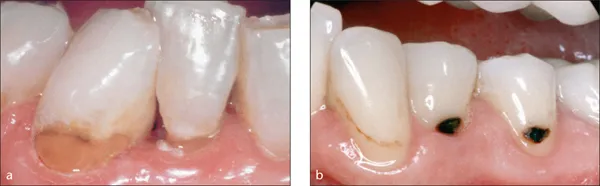
Abb. 18-2a und b Für eine valide Einschätzung der Läsionsaktivität ist die Korrelation der Oberflächentextur und des Abstandes zum Gingivalsaum mit dem Infektionsgrad relevant. Während die Defekte in der Abb. 18-2a alle als aktiv eingeschätzt werden mussten, war bei der Patientin in Abb. 18-2b der bukkale Defekt an Zahn 35 inaktiv, da er bei der Sondierung eine harte Oberfläche zeigte und in deutlichem Abstand zum Gingivalsaum lag
Generell muss daher für den Praxisalltag empfohlen werden, mit einer Sonde nach fraglichen Defekten zu fahnden, indem vor allem im Approximalraum die Schmelz-Zement-Grenzen abgetastet werden. Im Gegensatz zur Detektion von Schmelzkaries, wo eine spitze zahnärztliche Sonde keinesfalls mit Druck eingesetzt werden soll20, bleibt damit bei Wurzelkaries die Sonde für die Detektion und Einschätzung der Aktivität der Läsionen das Mittel der Wahl. Dies gilt insbesondere in klinisch nicht einsehbaren Bereichen.
Die Anfertigung von Röntgenaufnahmen ist demgegenüber nur von sehr begrenztem Nutzen bei der Läsionsdetektion, da Initialdefekte oft nicht von zervikalen Radioluzenzen (Burnout-Effekten) unterschieden werden können (Abb. 18-3). Erst größere Demineralisationsdefekte sind sicher röntgenologisch darstellbar, können dann aber auch klinisch mühelos sondiert werden.
Zahlreiche mikrobiologische Studien haben gezeigt, dass Wurzelkariesläsionen von einem Biofilm erzeugt werden können, der vermehrt Mutans-Streptokokken und Laktobazillen aufweist. Abgesehen davon, dass diese Kariespathogene vermehrt in entsprechenden Defekten gefunden werden und dass bei Trägern von Wurzelkaries im Vergleich zu Gesunden auch eine erhöhte Konzentration an spezifischen Antikörpern ermittelt werden kann, weisen diese Kariespathogene eine Reihe von Virulenzfaktoren auf, wie z. B. die Fähigkeit zur Säurebildung und Säuretoleranz, zur Bildung extrazellulärer Polysaccharide als Strukturmerkmal des Biofilms und zur Produktion von Bakteriozinen. Zusätzlich gibt es auch immer mehr Hinweise darauf, dass Aktinomyzeten und hier vor allem die virulente Subspeziesgruppe A. viscosus als ätiologischer Faktor eine Rolle spielen44. Betont werden muss aber, dass nicht einzelne Bakterien Wurzelkaries erzeugen, sondern dass aus der Inter...
Inhaltsverzeichnis
- Couverture
- Page de titre
- Copyright
- Verzeichnis der Autoren
- Inhaltsverzeichnis
- Teil I Das Alter
- Teil II Allgemeinerkrankungen im Alter
- Teil III Die alternde Mundhöhle und ihre Erkrankungen
- Teil IV Gerostomatologische Therapie
- Teil V Praxisorganisation und rechtliche Aspekte
- Sachregister
Häufig gestellte Fragen
Ja, du kannst dein Abo jederzeit über den Tab Abo in deinen Kontoeinstellungen auf der Perlego-Website kündigen. Dein Abo bleibt bis zum Ende deines aktuellen Abrechnungszeitraums aktiv. Erfahre, wie du dein Abo kündigen kannst
Nein, Bücher können nicht als externe Dateien, z. B. PDFs, zur Verwendung außerhalb von Perlego heruntergeladen werden. Du kannst jedoch Bücher in der Perlego-App herunterladen, um sie offline auf deinem Smartphone oder Tablet zu lesen. Erfahre, wie du Bücher herunterladen kannst, um sie offline zu lesen
Perlego bietet zwei Abopläne an: Elementar und Erweitert
- Elementar ist ideal für Lernende und Profis, die sich mit einer Vielzahl von Themen beschäftigen möchten. Erhalte Zugang zur Basic-Bibliothek mit über 800.000 vertrauenswürdigen Titeln und Bestsellern in den Bereichen Wirtschaft, persönliche Weiterentwicklung und Geisteswissenschaften. Enthält unbegrenzte Lesezeit und die Standardstimme für die Funktion „Vorlesen“.
- Pro: Perfekt für fortgeschrittene Lernende und Forscher, die einen vollständigen, uneingeschränkten Zugang benötigen. Schalte über 1,4 Millionen Bücher zu Hunderten von Themen frei, darunter akademische und hochspezialisierte Titel. Das Pro-Abo umfasst auch erweiterte Funktionen wie Premium-Vorlesen und den Recherche-Assistenten.
Wir sind ein Online-Lehrbuch-Abo, bei dem du für weniger als den Preis eines einzelnen Buches pro Monat Zugang zu einer ganzen Online-Bibliothek erhältst. Mit über 1 Million Büchern zu über 990 verschiedenen Themen haben wir bestimmt alles, was du brauchst! Erfahre mehr über unsere Mission
Achte auf das Symbol zum Vorlesen bei deinem nächsten Buch, um zu sehen, ob du es dir auch anhören kannst. Bei diesem Tool wird dir Text laut vorgelesen, wobei der Text beim Vorlesen auch grafisch hervorgehoben wird. Du kannst das Vorlesen jederzeit anhalten, beschleunigen und verlangsamen. Erfahre mehr über die Funktion „Vorlesen“
Ja! Du kannst die Perlego-App sowohl auf iOS- als auch auf Android-Geräten nutzen, damit du jederzeit und überall lesen kannst – sogar offline. Perfekt für den Weg zur Arbeit oder wenn du unterwegs bist.
Bitte beachte, dass wir Geräte, auf denen die Betriebssysteme iOS 13 und Android 7 oder noch ältere Versionen ausgeführt werden, nicht unterstützen können. Mehr über die Verwendung der App erfahren
Bitte beachte, dass wir Geräte, auf denen die Betriebssysteme iOS 13 und Android 7 oder noch ältere Versionen ausgeführt werden, nicht unterstützen können. Mehr über die Verwendung der App erfahren
Ja, du hast Zugang zu Der alte Patient in der zahnärztlichen Praxis von Frauke Müller,Ina Nitschke im PDF- und/oder ePub-Format sowie zu anderen beliebten Büchern aus Medizin & Zahnmedizin. Aus unserem Katalog stehen dir über 1 Million Bücher zur Verfügung.