![]()
Vorwort zur 1. Auflage
Dieses Buch ist aus einer Fortbildungsreihe entstanden, die der Verfasser 2005 und 2006 in regelmäßigen Abständen für seine Assistenten abgehalten hat. Ziel war eine Wiederholung des Examenswissens über die Gerinnung und ihre klinischen Implikationen. Gleichzeitig sollte auch eine Aktualisierung der Fortschritte der letzten Jahre geliefert werden.
Was zunächst als kleine Broschüre für den Hausgebrauch geplant war, wuchs dann schließlich zu dieser Einführung, die so – wie ich hoffe – dem Studenten und dem Assistenten gleichermaßen hilfreich sein möge.
Die historischen Exkurse sollen auf die lange Tradition der Hämostaseologie verweisen und sollen nicht nur der Auflockerung dienen, sondern auch den Respekt vor den Hämostaseologen bezeugen, die mit bewundernswerten Experimenten das faszinierende System der Gerinnung aufgeklärt haben.
Für vielfältige Hilfe bei der Abfassung des Manuskriptes bedanke ich mich bei Frau Erika Leveringhaus sehr herzlich, die sich mit unermüdlichem Fleiß durch die ungewohnte Materie gekämpft hat. Bei Frau Susanne Soer bedanke ich mich für die Hilfe bei der Herstellung der Schemazeichnungen und der Illustrationen. Mein Dank geht ebenfalls an Herrn Manfred Job, MA, Lehrstuhl für Ethik und Geschichte der Medizin der Ruhr-Universität Bochum, für die Hilfe bei der Beschaffung vieler medizinhistorischer Artikel.
| Bochum, August 2007 |
Herbert A. Neumann |
![]()
1 Einleitung
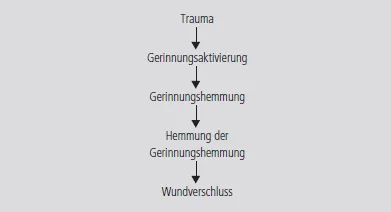
Das Gerinnungssystem besteht aus Substraten, Proenzymen, Enzymen, Coenzymen, Mediatoren, Thrombozyten und dem Gefäßendothel. Die Aktivierung des Gerinnungssystems erfolgt schnell und ohne hohen Energieaufwand über enzymatische Prozesse, meist Proteolysen. Das Zentralereignis ist die Bildung von Fibrin aus Fibrinogen nach Kontakt von Blut mit verletztem Gewebe. Im Falle einer Verletzung kommt es bei den größeren Gefäßen zur Gefäßkontraktion und Thrombenbildung. Da die Kapillaren keine Muskulatur besitzen, erfolgt hier die Blutungsstillung lediglich durch die Thrombenbildung. Parallel zum Gerinnungssystem existiert ein lytisches System, das unter physiologischen Bedingungen das Gerinnungssystem quantitativ leicht überwiegt, sodass das Blut optimal fließen kann. Im Falle einer Verletzung werden Endothel, Thrombozyten und plasmatische Gerinnungsfaktoren innerhalb kürzester Zeit aktiviert. Der Ablauf der Gerinnung wurde als Wasserfall oder auch als Kaskade von Reaktionen oder auch als Wasserfall-Kaskaden-Modell bezeichnet [8, 22, 23]. Schon während des Gerinnungsablaufes wird das lytische System aktiviert, um eine Ausbreitung des Gerinnungsprozesses zu verhindern und um diesen auf den Ort der Läsion zu reduzieren (Abb. 1). Diese Abläufe werden durch komplexe Aktivierungs-, Initiations- und Amplifikationsreaktionen sowie Inaktivierungsprozesse reguliert.
Abbildung 1 Ablauf der Blutgerinnung
![]()
2 Das Endothel
Struktur und allgemeine Funktionen
Das Endothel ist eine selektive Schranke zwischen Blutstrom und Gefäßwand für gelöste Substanzen, Makromoleküle und Zellen. Es kontrolliert aktiv den Austausch zwischen Gefäßlumen und Interstitium. Das Endothel reguliert den Gefäßtonus, z. B. durch den Vasokonstriktor Endothelin-1. Es spielt eine wichtige Rolle für die Interaktion von Leukozyten mit der Gefäßwand, z. B. im Rahmen von Entzündungen. Veränderungen des Blutflusses, mechanisch oder metabolisch, werden vom Endothel registriert und weitergeleitet. Es synthetisiert eine große Zahl von Mediatoren und kann deshalb als großes endokrines Organ angesehen werden. Neben seinen Aufgaben als Gefäßregulator nimmt es eine zentrale Rolle im Gerinnungsprozess ein und hat teil sowohl an gerinnungsfördernden als auch an gerinnungshemmenden Prozessen [17].
Eine wichtige Funktion der Endothelien für die Optimierung der Fließeigenschaften des Blutes beruht auf seiner leicht negativen Ladung. Da auch die Thrombozyten und die Erythrozyten eine leicht negative Ladung besitzen, ermöglichen die elektromagnetischen Abstoßungskräfte einen reibungsfreien Fluss der zellulären Partikel des Blutes. Die Partikel fließen normalerweise laminar, wobei die Fließgeschwindigkeit der im Blut schwimmenden Partikel in der Mitte schneller ist als in der Nähe der Gefäßwand. Durch die gleichpolige Ladung entsteht ein dünner Plasmafilm zwischen Zellen und Endothel, sodass in der Regel die zellulären Bestandteile des Blutes nicht mit dem Endothel in Kontakt kommen.
Lösliche Substanzen und Makromoleküle können durch das Endothel diffundieren, indem sie sich zwischen den Zellen des Endothels bewegen. Eine weitere Möglichkeit des Stoffaustausches im Endothel ist die transzelluläre Bewegung in zytoplasmatischen Vesikeln. Bei Entzündungen oder Verletzungen nimmt die Permeabilität des Endothels zu. Ausgelöst wird dies durch Histamin, Serotonin, Thrombin und Bradykinin. Durch diese Mediatoren kommt es zu Lücken zwischen den Endothelzellen und damit zu einer unselektiven Extravasion von Makromolekülen und Wasser und somit zum Gewebsödem, das sich klinisch durch Schwellung, Rötung und Druckschmerzhaftigkeit manifestiert [3, 4, 5, 31].
Bei Entzündungsvorgängen wandern durch Vermittlung von Zytokinen Leukozyten in die Gefäßwände und das umgebende Gewebe ein und werden mithilfe von sogenannten Selectinen an das Endothel gebunden. In einem weiteren Schritt werden die Leukozyten durch Adhäsionsmoleküle (ICAM) zusätzlich stärker an das Endothel gebunden. Durch Sekretion von Proteasen werden die Endothelien aufgelöst und die Leukozyten wandern in das umgebende Gewebe. Diese Abläufe spielen auch für die Entstehung der Arteriosklerose eine wichtige Rolle.
Sobald es zu einer Gewebsverletzung kommt und subendotheliale Strukturen mit den Bestandteilen des Blutes in Verbindung kommen, wird der Gerinnungsprozess eingeleitet. Grob eingeteilt, kommt es zu folgenden Reaktionsschritten der Blutgefäße:
Die erste Reaktion auf ein Trauma ist die nervale Endothelin-1- und Adrenalin-vermittelte Vasokonstriktion mit dem Ziel einer Drosselung der Blutgefäße. Endothelin wird unmittelbar nach der Verletzung freigesetzt und führt zur Kontraktion der Gefäße. Das Endothel produziert eine große Zahl von gerinnungsaktivierenden Substanzen.
Weiterhin wurde beobachtet, dass Kapillaren und kleine Venolen spontan kollabieren und weiterhin durch Extravasate in das Gewebe tamponiert werden und so den Blutfluss hemmen [6, 22].
Thrombotische Funktionen des Endothels
Durch Freisetzen von thrombogenen Faktoren kommt es zur Bildung eines zunächst überwiegend aus Thrombozyten bestehenden Thrombus. Die Endothelfaktoren, die eine thrombotische Wirkung induzieren, sind:
– der von-Willebrand-Faktor (s. dort)
– das Thromboplastin, auch Faktor III oder Gewebsfaktor genannt, ein wichtiger Aktivator der plasmatischen Gerinnung aus dem Subendothel (s. Kap. Plasmatische Gerinnung)
– der Faktor V (s. Kap. Plasmatische Gerinnung)
– der platelet-activating factor (PAF)
– das high-molecular-weight kininogen (HMWK), auch genannt Faktor XIV oder Fitzgerald-Faktor (s. Kap. Plasmatische Gerinnung)
– das Kollagen
– der Plasminogenaktivatorinhibitor-1 (PAI-1) = Hemmer der Fibrinolyse (s. dort).
Das Endothel exprimiert Rezeptoren für
– das HMWK
– die Tenase (s. dort)
– die Prothrombinase (s. dort)
– den Faktor IX und X (s. Kap. Plasmatische Gerinnung)
– den von-Willebrand-Faktor (s. dort)
– das Fibrinogen.
Über diese Rezeptoren binden die entsprechenden Faktoren an das Endothel am Ort der Läsion. Zusätzlich bindet das Endothel Fibrinogen, Fibronektin und Thrombin [5, 16].
Antithrombotische Funktionen des Endothels
Parallel zu den thrombotischen Endothelfaktoren werden im Endothel auch antithrombotische Mediatoren synthetisiert und aktiviert:
– tissue factor pathway inhibitor (TFPI; s. Kap. Gerinnungssystem)
– tissue type plasminogen activator (t-PA), wird im Endothel synthetisiert und sezerniert (s. Kap. Fibrinolyse)
– Stickstoffmonoxid (NO) = Aggregationshemmer
– Prostacyclin (PGI2), das antiaggregatorisch wirkt und durch Thrombin und Noradenalin stimuliert wird, hemmt die Thrombozytenaktivierung
– ADPase, hemmt den Aktivator ADP, einen zentralen Stimulator der Thrombozytenaggregation
– Thrombomodulin, welches Thrombin bindet, somit dessen enzymatische Spezifität verändert und dadurch das Protein C aktiviert (s. Kap. Plasmatische Gerinnung)
– Protein S, Cofaktor des Proteins C (s. Kap. Gerinnungshemmung)
– vasodilator-stimulated phosphoprotein (VASP) [24].
Eine weitere Funktion für die gerinnungshemmende Wirkung de...